COVID-19
COVID-19 に関する最新の情報は内閣官房ホームページをご参照ください
医療器機製造業に必要な書類
医療器機の製造業は登録申請です。
ですから書類が揃って間違いがなく、かつ責任技術者の要件に間違いがなければ簡単に取得できます。
最初に登録申請書を記入します。
ただし、これは電子申請しか受付けない県と紙の書類でも受付ける都府県があります。
今回は、紙の方でご説明します。
電子申請はとても面倒なので、近日中に動画でご説明します。
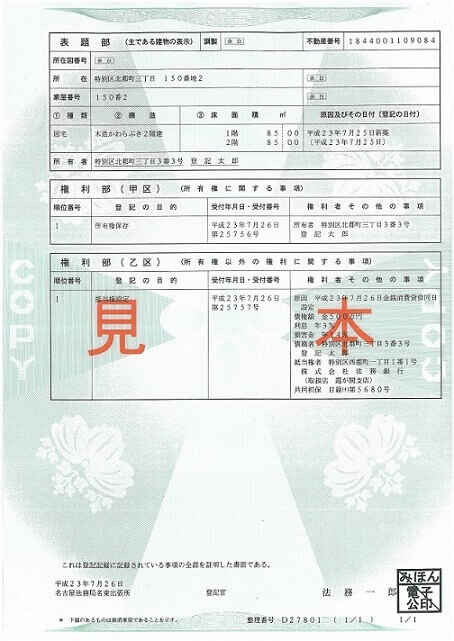
先ず、登録申請書ですが以下のような書類です。
ご覧の通りなんてことはありません。
私の会社は、製造業を取得していませんから、これはあくまでも見本です。
次に、他の書類です。
必要な書類は以下の通りですが、都道府県によって、微妙に異なります。
私は、北からいうと、青森、秋田、石川、福井、長野、埼玉、東京、神奈川、兵庫でお手伝いをしました。
ちなみに東京の場合、都庁ではなく東京都健康安全研究センターに届けます。
書類そのものは同じですが、記入する内容が微妙に異なるのです。
とは言え、間違っていれば修正箇所を教えてくれます。
難しい申請ではありません。
ただし、窓口の担当者は、その対応がかなり違います。
とても、親切な人と「ムカッ!」と来るような人がいます。
そこは、大人の対応で凌いで下さい。
登記事項証明書(登記簿謄本)
申請日から6ヶ月以内に発行されたものを添付
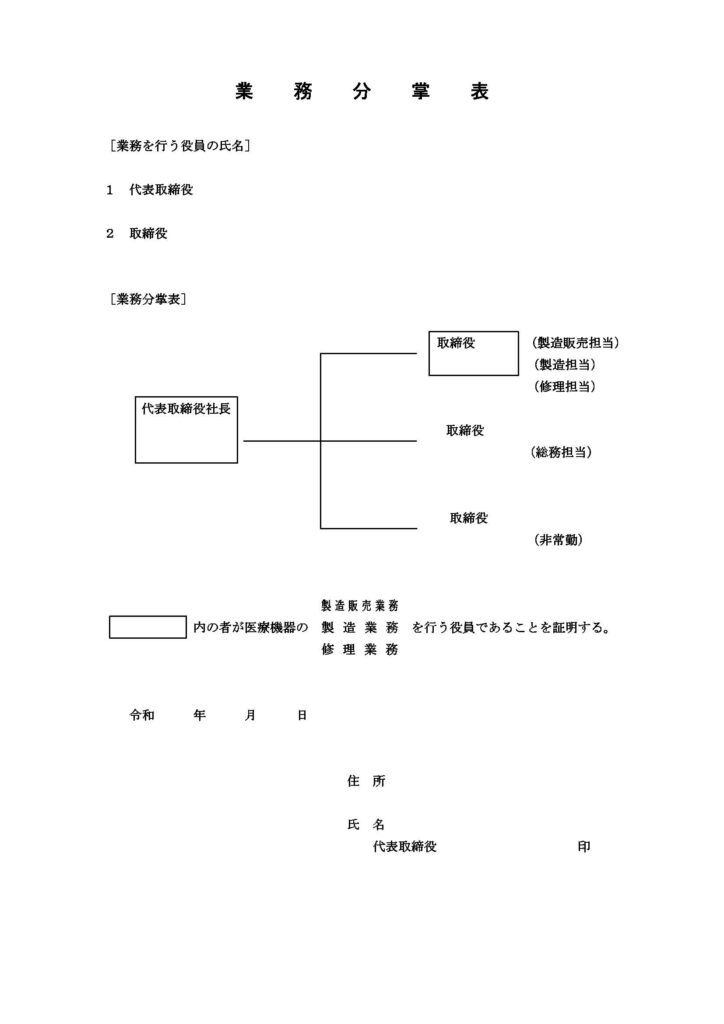
役員の業務分掌表
登記された役員全員が「業務を行う役員」に該当する場合は添付不要です。
ウ 申請者が欠格条項に該当するか否かに関する診断書もしくは疎明書
「業務を行う役員」について、申請日より3ヶ月以内に診断もしくは疎明されたものを添付
社長の診断者と他に関係する役員がいる場合は、その人の疎明書があればそれでOKです。
ただし、場所によって、全員の診断書を要求されることもあります。
普通の医療機関(町の病院・クリニック)で診断書を書いて貰うと5,000円程度します。
※疎明書とは
「疎明対象の役員が欠格条項に該当しないこと」を本人、または法人の代表取締役が証明する文書です。
社長以外の役員の場合、本人よりも社長が疎明した方が良いと思います。
責任技術者・製造管理者の「雇用契約書の写し」又は「雇用及び使用関係を証する書類」
例えば社長が責任技術者の場合、自分の名前で自分を雇っていることを書面にして下さい。
例えば、私の場合販売業ですが、一人でやってます。よって以下のような証明書になります。
責任技術者・製造管理者の資格を証する書類
高度管理医療機器又は管理医療機器を製造する製造所
(1)大学等で、物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医 学又は歯学に関する専門の課程を修了した者
(2)旧制中学若しくは高校又はこれと同等以上の学校で、物理学、化学、生物学、工学、情 報学、金属学、電気学、機械学、薬学、医学又は歯学に関する専門の課程を修了した後、 医療機器の製造に関する業務に三年以上従事した者
(3)医療機器の製造に関する業務に五年以上従事した後、別に厚生労働省令で定めるところ により厚生労働大臣の登録を受けた者が行う講習を修了した者
※ この講習会は、「財団法人医療機器センター」で行われています。
(4)厚生労働大臣が前三号に掲げる者と同等以上の知識経験を有すると認めた者資格要件に該当するかご不明な場合は医療機器審査担当にお問い合わせください。
註:一番下の(4)は、認められることがないと思った方が良いと思います。
ゼロではないですが、どんな人が上記に該当するのか分かりません。
一般医療機器のみを製造する製造所
(1) 旧制中学若しくは高校又はこれと同等以上の学校で、物理学、化学、生物学、工学、情 報学、金属学、電気学、機械学、薬学、医学又は歯学に関する専門の課程を修了した者
(2)旧制中学若しくは高校又はこれと同等以上の学校で、物理学、化学、生物学、工学、情 報学、金属学、電気学、機械学、薬学、医学又は歯学に関する科目を修得した後、医療機 器の製造に関する業務に三年以上従事した者
(3)厚生労働大臣が前二号に掲げる者と同等以上の知識経験を有すると認めた者。
資格要件に該当するかご不明な場合は医療機器審査担当にお問い合わせください。
医療機器の製造工程のうち設計のみを行う製造所
(1)前二項に該当する者もしくは、製造業者が設計に係る部門の責任者として指定する者
体外診断用医薬品を製造する製造所
(1) 薬剤師
製造所の場所を明らかにした図面
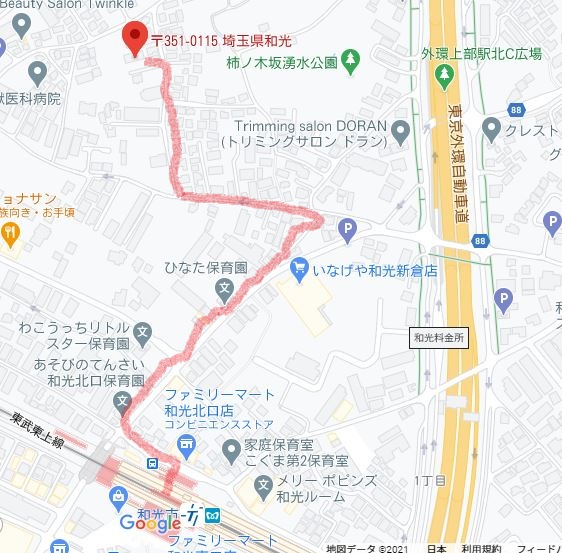
(1)案内図
最寄り駅からの案内図です。
GoogleMapを切り取って、道路の部分に線を引いて下さい。
(2)建物の配置図
同一地番内に複数の建物がある場合に添付
建物内の一部に製造所がある場合は、フロア全体図も添付
(3)製造所の平面図
登録対象となる製造所の範囲がわかるもの
これはサンプルがありませんが、普通の配置図と平面図です。
ISO13485:2016+QMS省令対応の品質マニュアルのお求めは、上の画像をクリックして下さい。