ISO13485(医療機器-品質マネジメントシステム)とはは何か?
ISO13485(医療機器-品質マネジメントシステム)とは、「医療機器の安全性と品質の維持」をねらいとした国際規格です。
全てとは言いませんが、多くの医療機器は人の健康や病気の治療に直接的な影響を与えます。
医療ISO13485は、医療機器の設計、製造、据付及び付帯サービス並びに関連するサービスにたずさわる組織を対象とした内容になっています。
規格構成はISO9001をベースとしており、そこに医療機器に関する安全性と有効性及び品質を確保するために必要な規制目的のための要求事項が盛り込まれています。
俗な言い方ですが、ISO9001+医療機器の特殊性
医療機器用にグレードアップされた品質マネジメントシステム、それがISO13485だと言って良いと思います。
ISO13485を理解しようとして、「ISO13485:2016」を購入した方は、その多くが冒頭の数ページを読んで挫折すると思います。
翻訳している方に失礼なので、翻訳が悪いとはいいませんが、規格の文章はあまりに固く、法律文章のような言い回しで、読みにくいのです。
今、ご覧頂いている、ワークシフトのWebサイトでは、これまでに何度も「ISO13485を理解する」と題して、規格の文章をかみ砕いてご紹介しました。
かみ砕くことで、正確性は多少損なわれますが、読み手の理解を促進することはできます。
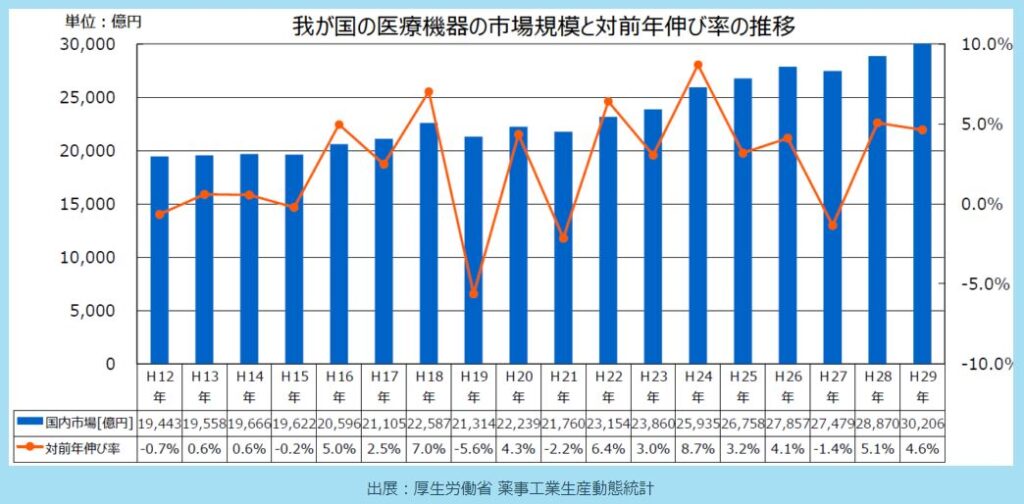
下のグラフをご覧ください。
国内の医療機器市場規模は、2004年以降、増加に転じ、2兆円超で推移。2010年代後半には約3兆円となり、過去最大の市場規模となっています。国内の医療費は、2016年度は42.1兆円。医療機器市場は、うち約7%となっています。
日本の医療機器市場の動向としては2010年代後半には約3兆円で過去最大の市場規模となっています。
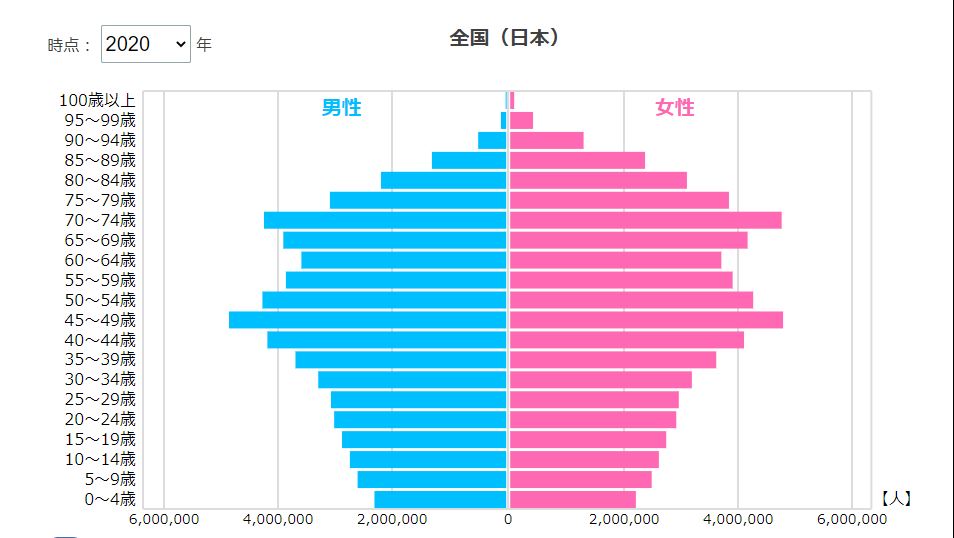
また、下の人口ピラミッドの形をみれば、団塊の世代と呼ばれる、人口が多い世代が、今後、医療機器や病院のお世話になる年齢に達します。
そこから考えると、下のグラフから、15年後くらいが、国内医療機器市場のピークになることが予想されます。
(グラフは2020年なので、2022年時点から12~15年後くらいです)
品質マネジメントシステムは必須
医療機器を作って、上市するためには、その組織(企業・会社)が、医療機器に関する品質マネジメントシステムを備えていなければなりません。
ISO13485の取得は、国内だけで医療機器を製造・販売するなら必要なものではありませんが、厚生労働省のQMS省令はISO13485に準拠しています。
逆に、厚生労働省のQMS省令は、医療機器を製造・販売するために、必ず必要な品質マネジメントシステムです。
必要な費用が大きく異なるので、そこは、経営者様の判断になりますが、海外でも販売を狙うなら、ISO13485、国内市場だけを狙うなら厚生労働省のQMS省令。
実際の品質マネジメントシステムは、ほとんど同じですから、よく考えて対応を決めれば良いと思います。
ちなみに、必要な費用は、
ISO13485=200万円程度(審査期間に払う費用)
厚生労働省のQMS省令=第一種で15万円程度です。
準備期間は、半年と考えれば十分
繰り返しますが、ISO13485でも、厚生労働省のQMS省令でも社内で準備すべきことはほとんど同じです。
QMSマニュアルをつくり、手順書や記録の様式を準備する。
マニュアルや手順を社員に周知徹底して、教育を行う。
内部監査を行って、マニュアル通り作業が進められているかをチェックする。
問題があれば、改善する。
改善には、教育もありますし、手順書の見直しもあります。
そして、上記を繰り返します。
それが、PDCAです。