医療機器製造販売業許可取得のための5役とは
新規で、医療機器業界への参入を狙って、医療機器の製造販売業を取得しようとすると、大きな壁があります。
それが薬事3役の有資格者が社内にいるかどうかです。
薬事5役という言い方もありますが、管理監督者と管理責任者は、経営者がその職務を負うので、特に問題になりません。
学歴や経験年数なども求められません。
ですから、管理監督者と管理責任者のことは、最後に軽く触れる程度で説明します。
医療機器製造販売業許可を取得するために設置が求められる5役は以下の通りです。
- 医療機器等総括製造販売責任者
- 国内品質業務運営責任者
- 安全管理責任者
- 管理監督者
- 管理責任者
上記の中で総括製造販売責任者は、学歴だけでも要件を満たすので、比較的要件を満たしやすいです。
国内品質業務運営責任者や安全管理責任者は、実務経験が必要なので、新規で医療機器製造販売業に進出しようとする企業には厳しい要件です。
実務経験や学歴などは、しっかり確認されますから、そのつもりで証明する書類を準備してください。
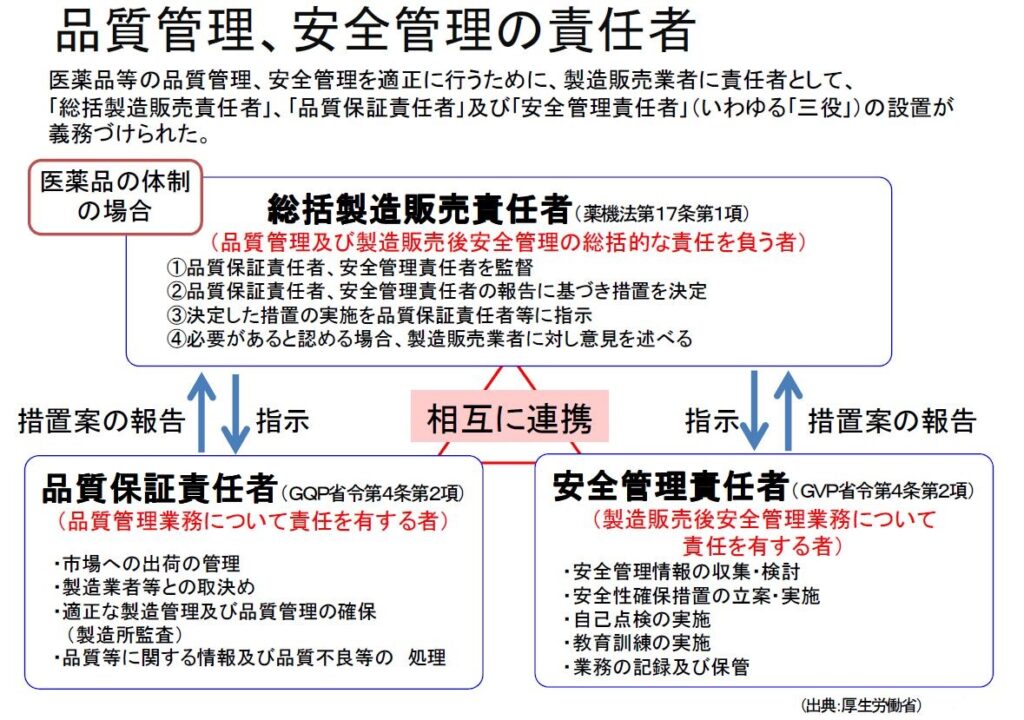
また、3役の業務関係は以下の図を参照にしてください。
以下、順番に見ていきましょう。
総括製造販売責任者
要件:専門科目は、30単位以上必要です。
| 施行規則第114条の49第1項 <高度管理医療機器> <管理医療機器>第1種・第2種製造販売業 |
1号 | 大学等で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学、歯学のいずれかの専門課程を修了した者 |
| 2号 | 旧制中学若しくは高校又は同等以上の学校で物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学、歯学のいずれかの専門課程を修了後、医薬品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に3年以上従事した者 | |
| 3号 | 医薬品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に5年以上従事後、総括製造販売責任者講習会を修了した者 | |
| 4号 | 上記と同等の知識経験があると厚生労働大臣の認めた者 | |
| 施行規則第114条の49第2項 <一般医療機器>第3種製造販売業 |
1号 | 旧制中学若しくは高校又はこれと同等以上の学校で、物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学に関する専門の課程を修了した者 |
| 2号 | 旧制中学若しくは高校又はこれと同等以上の学校で、物理学、化学、生物学、工学、情報学、金属学、電気学、機械学、薬学、医学又は歯学に関する科目を修得した後、医薬品、医薬部外品、化粧品、医療機器又は再生医療等製品の品質管理又は製造販売後安全管理に関する業務に3年以上従事した者 | |
| 3号 | 厚生労働大臣が前2号に掲げる者と同等以上の知識経験を有すると認めた者 |
医療機器の製造販売業者は、医療機器の品質管理及び製造販売後安全管理を行うものとして、総括製造販売責任者を置かなければならないとされ(薬事法第17条第1項)、その基準が定められています(薬事法施行規則第85条)。
また、製造業者は、医療機器の製造を実地に管理させるために製造所ごとに責任技術者を置かなければならないとされ(薬事法第17条第5項)、その資格要件が定められています(薬事法施行規則第91条)。
ただし、実際の業務は、国内品質業務運営責任者と安全管理責任者が行います。
総括製造販売責任者は、その管理や書類の承認を行う役目なので、業務そのものはそれほどありません。
(薬務課の人に怒られそうですが、実際の話本当のことです)
国内品質業務運営責任者
国内品質業務運営責任者とは、医療機器の品質管理業務の責任者となり、市場への出荷判定や回収処理等を担当します。
品質管理業務には、知識経験が必要となるため、業務経験者を配置することが求められています。
(ベンチャー企業が、医療機器業界に参入するとき、これが障害になることが多いです)
国内品質業務運営責任者の資格要件は以下のすべての満たす必要があります。
① 製造販売業者における品質保証部門の責任者であること
② 品質管理業務その他これに類する業務に3年以上従事した者であること
③ 国内の品質管理業務を適正かつ円滑に遂行しうる能力を有する者であること
④ 医療機器等の販売に係る部門に属する者でないことその他国内の品質管理業務の適正かつ円滑な遂行に支障を及ぼすおそれがない者であること
色々、難しく書いてありますが、ようするに品質管理業務に類する業務を3年以上経験していれば良いのです。
では、その品質管理業務とは何か?
これも法律文書なので読みにくいですが
ア.管理監督者
イ.管理責任者
ウ.医療機器等総括製造販売責任者
エ.旧法下における品質保証責任者、製造管理者及び責任技術者
オ.その他製造販売業者又は製造業の製造管理又は品質管理に係る業務に従事した者等
カ.ISO 9001又はISO 13485の認証を受けた事業者等(製品の製造販売又は製造を行うものに限り、サービス提供等のみを行うものを除く。)に係る品質マネジメントシステムの継続的改善又は維持に係る業務に従事した者(第2種、第3種製造販売業者のみ)
また、「3年以上」とは、自社、他社を問わず該当する業務の合計年数でもよいこととされています。
第1種製造販売業の場合は、上のア~オだけです。
安全管理責任者
第1種医療機器製造販売業者の場合
以下のすべてを満たす者:
① 安全管理統括部門の責任者
② 安全確保業務その他これに類する業務に3年以上従事した者
③ 安全確保業務を適正かつ円滑に遂行しうる能力を有する者
④ 医薬品等の販売に係る部門に属する者でないことその他安全確保業務の適正かつ円滑な遂行に支障を及ぼすおそれがない者
(根拠法令:GVP省令第4条第2項)
第2種・第3種医療機器製造販売業者の場合
以下のすべてを満たす者:
① 安全確保業務を適正かつ円滑に遂行しうる能力を有する者
② 医薬品等の販売に係る部門に属する者でないことその他安全確保業務の適正かつ円滑な遂行に支障を及ぼすおそれがない者
(根拠法令:GVP省令第13条、第15条)
第1種の場合は安全管理統括部門を設置する必要があります。
また、安全管理責任者に3年の従事経験が求められています。
2種、3種には部門の設置および従事経験は求められていません。
上を見ると、要するにどんな要件? と思うはずです。
法律文書なので、「誰でも良い」とは書けないので難しく書いているだけです。
責任を持って、普通に仕事が出来る人なら誰でも良いのです。
言い換えると、2種、3種の場合、安全管理責任者に求められる経験も学歴もありません。
国内品質業務運営責任者および第1種製造販売業者の場合には安全管理責任者について、それぞれ3年の従事経験が求められています。
これは特に新規参入企業にとって厳しい要求事項です。
事業開始初期においては、要件を満たす方を雇い、計画的に後進を育成していく必要があります。
管理監督者・管理責任者
管理監督者・管理責任者に求められる学歴や経験の要件はありません。
会社の経営陣であれば問題ありません。
必要なリソースを管理し、動かすことが出来る人です。
難しく考えないでください。
それぞれの兼務
医薬品と医療機器のどちらも作っているときは、兼務が複雑になります。
今回は、医療機器だけを製造販売しているという前提で説明します。
| 第一種医療機器製造販売業者 | 総括製造販売責任者と国内品質業務運営責任者との兼務が可能です。 |
| 第二種医療機器製造販売業者 | 総括製造販売責任者と国内品質業務運営責任者との兼務を可能とするとともに、国内品質業務運営責任者を兼務していない場合に限り、総括製造販売責任者と安全管理責任者との兼務が可能です。 |
| 第三種医療機器製造販売業者 | 総括製造販売責任者、国内品質業務運営責任者及び安全管理責任者の三者の兼務が可能です。 |
| 製造業責任技術者 | 業務を行う事務所と同一施設内に製造所を有する場合には、国内品質業務運営責任者と責任技術者との兼務が可能です。 |
第一種製造販売責任者
法令要求上、資格要件を満たす者が2人いれば体制が組める訳です。
ただし、2人で支障なく業務を実施できることを当局に証明できなければなりません。
証明といっても、薬務課の調査で質問されたときに、答えられれば問題ありません。
あるいは、「今、立ち上げたばかりで、売上もありません。今後は、売上の伸びに応じて、人も増やし3役も個別に役職者を当てます」
といえば、どの都道府県自治体でも認めてくれます。
実際には医療機器専業企業の場合、管理監督者には社長が就くことが往々にしてあります。
社長は実質的に販売のトップですので、品責と兼務するのは現実的ではないでしょう。
必ず、質問されます。
第二種製造販売責任者
第2種の場合も第1種同様、法令要求上資格要件を満たす者が2人いれば体制構築が可能です。
しかし、ここでも薬務課の調査で色々質問されます。
第三種製造販売責任者
第3種の場合、法令上全ての役職を1人が兼務することは可能ですが、実質的に業務に支障が出ることと思われます。
複数人設置することが望ましいのですが、当初は仕方がありません。
薬務課の調査では、質問されますが、しっかり対応するといえば、法令上はできるのですから、それ以上は向こうもいいません。
まとめ
第1種、第2種、第3種のいずれにおいても、兼務しようとする役職において要求される資格要件等の条件等をすべて満していなければなりません。
また、業務に支障が生じない場合に限って兼務可能であるということです。